いろいろ 酸化 還元 電子 191719-酸化 還元 電子 覚え方
ールである.本稿では,酸化還元酵素のボルタンメトリーお よび脂質二分子膜を介した電子及びイオン移動ボルタンメト リーについて概説する. 2 酸化還元酵素のボルタンメトリー 2 1 触媒反応を伴わない酸化還元酵素のボルタンメト リーある酸化還元対の標準電位が大きな負の値をもつとき,還元体は強い還元剤になる.た とえば,Na/NaのE 0 = –271 Vなので,金属ナトリウムは強い還元剤である.アルカリ金 属やMgが電子供与体としてBirch還元やピナコール反応に用いられる根拠になっている酸化剤と還元剤との反応で,電子e-を含むイオン反応式のつくり方がよくわかりません。わかりやすく教えてください。 進研ゼミからの回答 こんにちは。いただいた質問について回答します。 質問内容 酸化剤と還元
酸化剤と還元剤 化学基礎 高校化学net参考書
酸化 還元 電子 覚え方
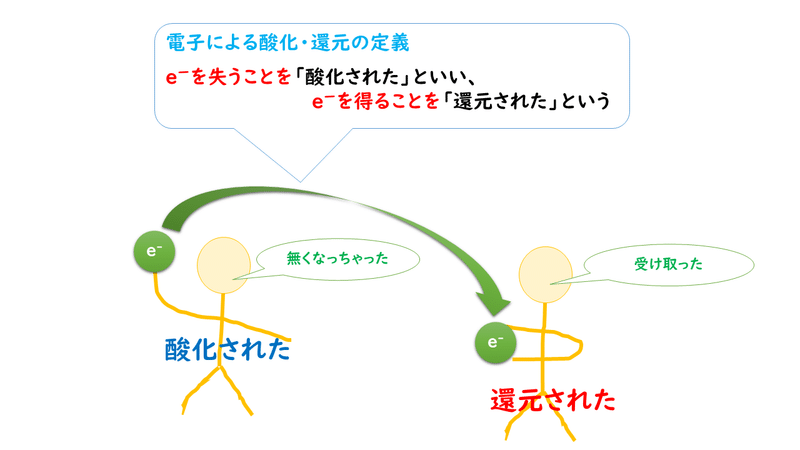
酸化 還元 電子 覚え方-そこで、酸化を、酸素との結合ということだけではな く、より広く、電子を失う反応を酸化ということにする。また、還元は酸化の逆反応であるから、電子 を受け取ることを還元と広く定義することにする。つまり、 酸化される = 電子(e−)を失うNh2, och3など電子供与基はドナー性を強くする。 azulene 038 v tcnq tcnqtcnq2還元されるとキノイド構造が6πのベンゼン環に戻って安定化する。 −は2つの電子吸引基の根元に出る。cn、no2など電子吸引基はアクセプター性を強くする。 1960 1970 1980 1990 00 有機



受験基礎化学 26 酸化還元反応 みかみの参考書ブログ
酸化還元電位と電子の授受および濃度の関係について、以下の式が成り立つ。 O ne R a a nF RT E E R o → = 0 ln 上式をネルンストの式と呼ぶ。O は酸化体、R は還元体、E0 は標準酸化還元電 位(または標準還元電位)である。この式を覚えておけば、面倒な符号酸化還元反応式は、そのとき酸化される物質が 電子 を放出する反応と、還元される物質が 電子 を受け取る反応に分けて記述する、すなわち 電子 を含む2つの反応式に分割して記述することができる。子酸化剤とが考えられる。一般に, Co3, Mn3, V5, Cu2 などを酸化剤とする研究が多く進められているが, これらの代表的な遷移金属イオンは酸化還元電位などの 検討により主に一電子酸化剤として働いていると考えら れる。すなわちマクロな反応としては,
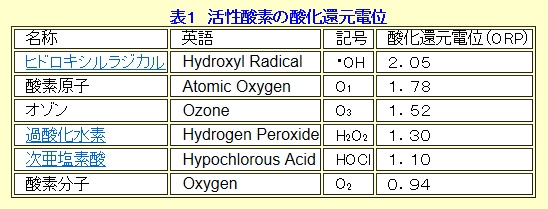
ORP)とは、ある酸化還元反応系における 電子 のやり取りの際に発生する 電位 (正しくは電極電位)のことである。 酸化還元反応とは電子の奪い合い 酸化還元反応とは、電子の奪い合いの反応のことです。 原子の外側に電子がビュンビュン飛んでいて、その外側の電子が奪われたり、うばったりする。 あれ?? 原子は電子を共有して結合するのではないの?酸化還元電位 (さんかかんげんでんい、Redox potentialもしくはOxidationreduction Potential;
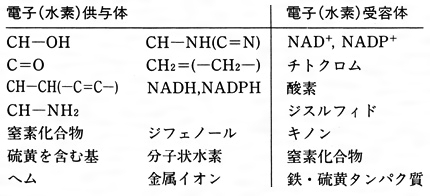
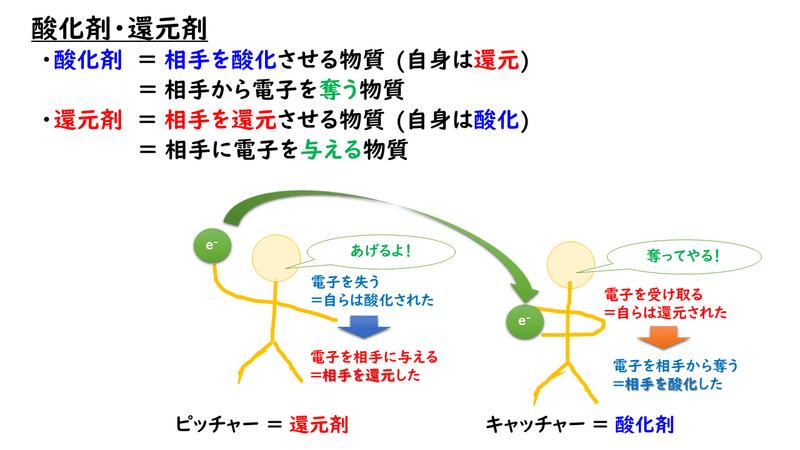
・酸化剤相手を酸化する(相手から 電子 を奪う)=自らは還元される(自らは 電子 を受け取る) ・還元剤相手を還元する(相手に 電子 を与える)=自らは酸化される(自らは 電子 を失う)電子還元と1電子還元の両方の能力をもっている。そのため、atp 合成にかかわる酸化還元 系では、この能力を生かして酸化還元反応を円滑に進める触媒として働き、極めて重要な役 割を果たしている。一方が還元されれば、もう一方は酸化されるんです。 こんな風に習いませんでした? 物質が酸素を得たら酸化で失ったら還元って。 これももちろん間違いじゃないんですけど。。 実は酸化還元って図1でも書きましたが水素の受け渡しや電子の受け渡しで




Senior High化学的化学基礎総復習ノートまとめ筆記 Clear



7 2 酸化数 おのれー Note
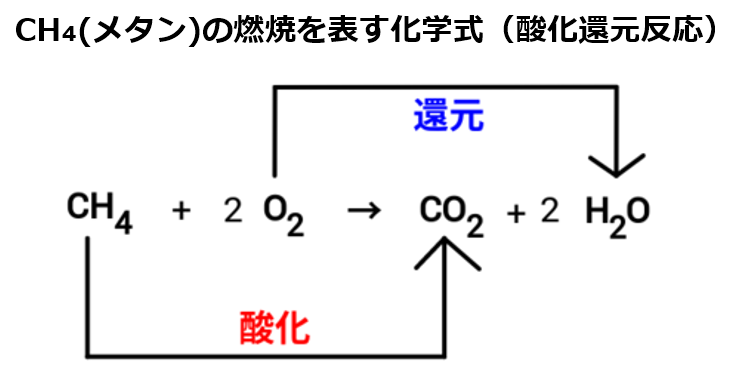
酸化還元電位を鑑みると、fad/fadh 2 <nad/nadhより、電子伝達系の反応は必ず酸化還元電位は大きくなると仮定すると、既に複合体Ⅰを介して進んでいる電子伝達系に、後からfad/fadh 2 由来の電子が系に入るのが予想できる。次に②酵素に結びつける。よく酸化還元反応と酸塩基反応をごちゃごちゃにしてしまうことがあるのですが、 酸化還元反応は電子の移動の反応であり、酸化還元電位に影響する 酸塩基反応はプロトン(H )の移動の反応であり、pHに影響する という決定的な違いがあります。酸化数 = 中性原子における価電子の数 - 所有している電子の数 ここで例 として、 メタン ch 4 の炭素原子 c の酸化数を考えてみます。 メタン ch 4 は、炭素原子 c を含んだ化合物の中で、炭素原子 c が最も還元された構造をしています。 炭素原子 c 近傍の電子密度は最大となっており、 その



酸化還元反応 電子のやり取り
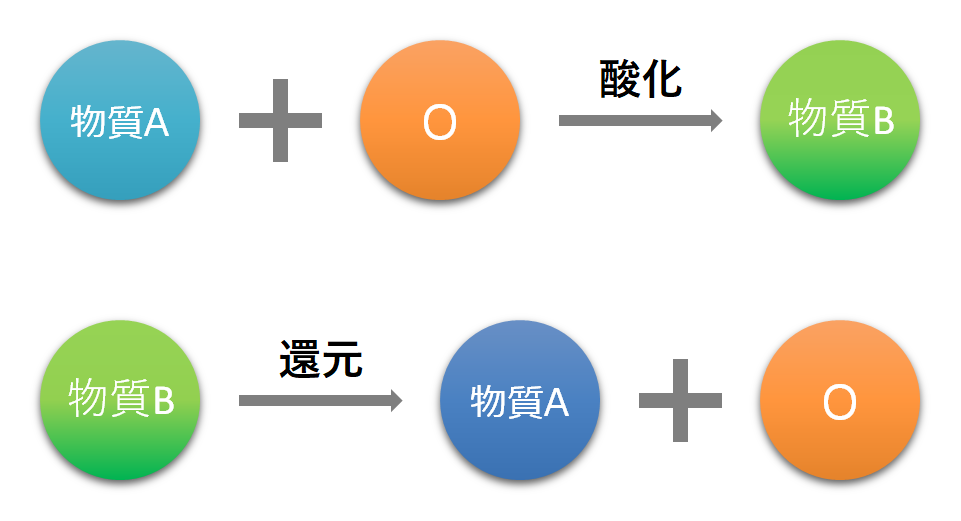



酸化と還元 酸化数から酸化還元反応を考えよう ふかラボ
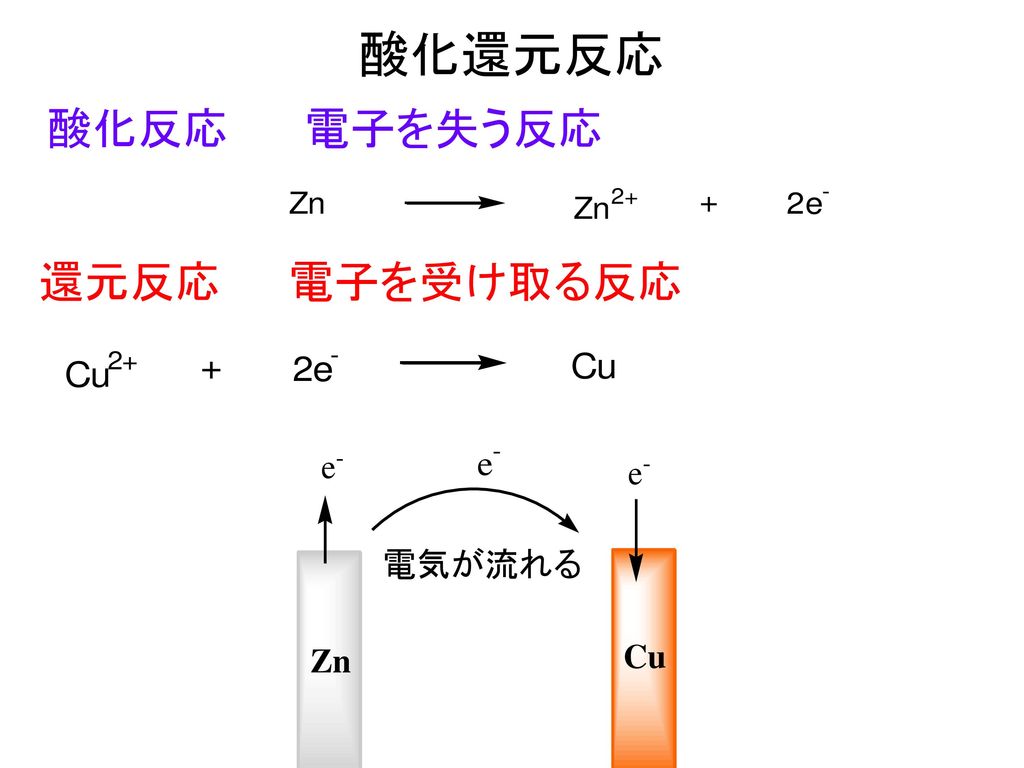
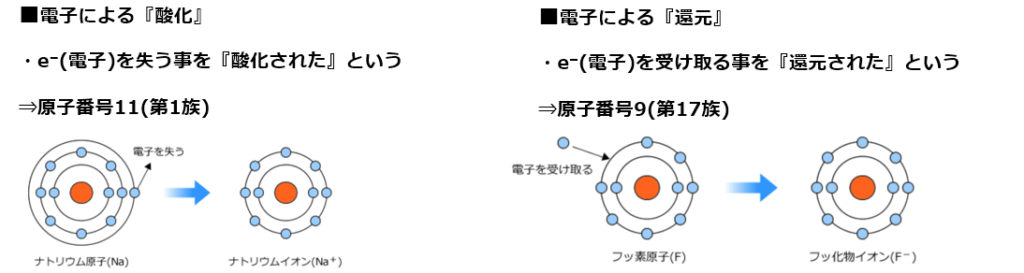
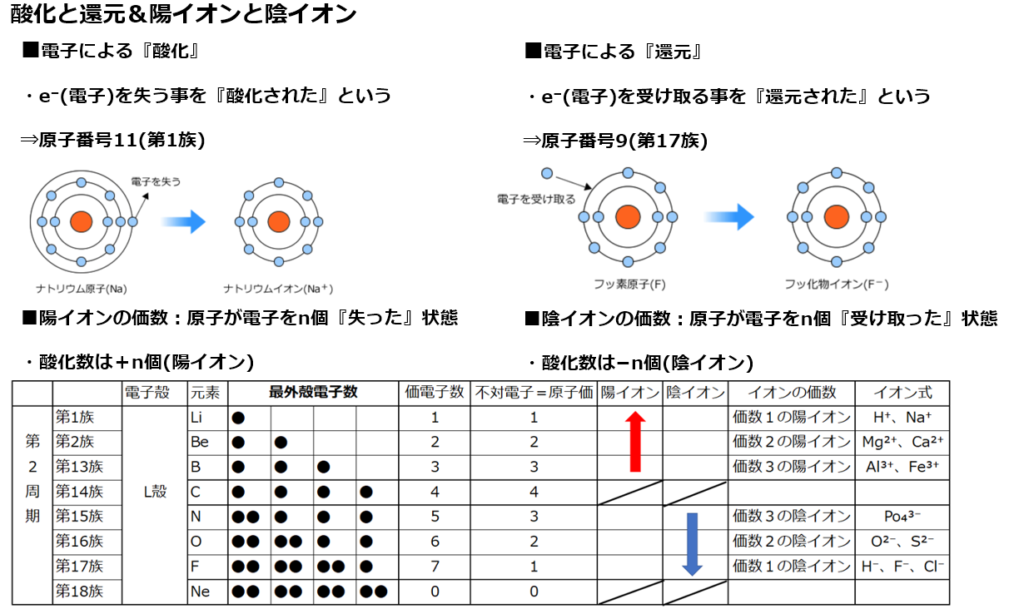
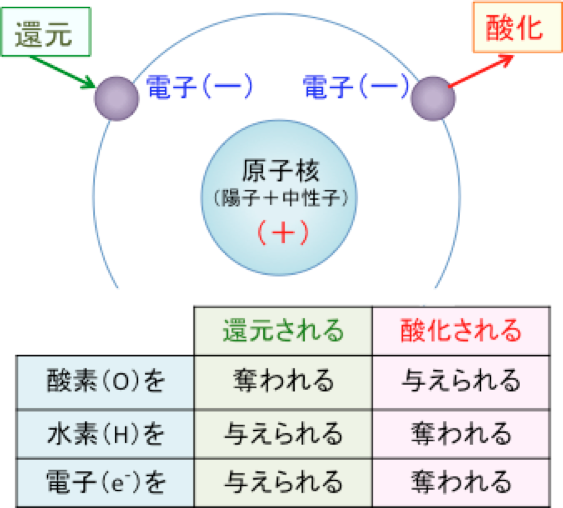
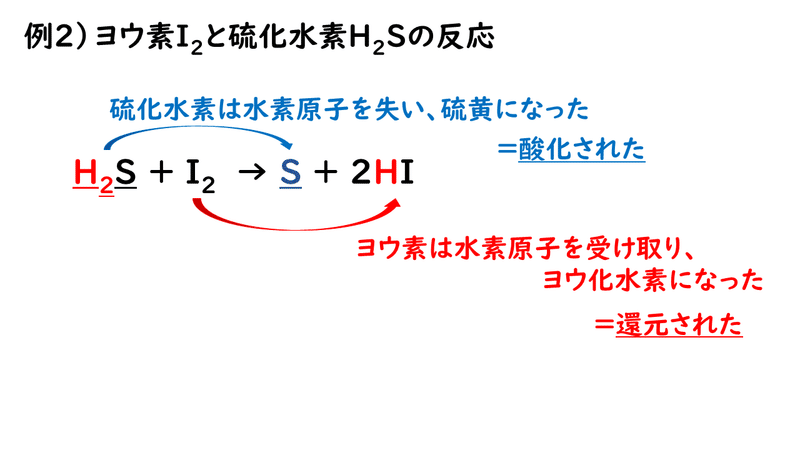
「酸化」 とは、「原子またはその原子を含む物質が 電子を失う 変化」です。 「還元」 とは、「原子またはその原子を含む物質が 電子を受け取る 変化」となります。 酸化と還元の関係 電子$\ce{e}$の出入りによって酸化と還元が変わるので,「酸化」と「還元」は 対 (つい) になる反応であることが分かります. このことから 酸素Oを失う反応は「還元」 水素Hを失う反応は「酸化」 ということになります.それぞれ電子を e - を用いた反応式で表せ。 (3) 豆電球が点灯しているとき,この電池で酸化される物質と還元される物質をそれぞれ記せ。 (4) 豆電球が点灯しているとき,電子は導線内をどちらの向き




代購代標第一品牌 樂淘letao 自然還元研究所hs 413dw Orpメーター酸化還元電位計



電池の化学 電池とは化学反応によってエネルギーを 直接に 直流 電力に変換する装置 燃焼 化学反応 熱エネルギー 電池 化学反応 Ppt Download
物質が電子e – を失うことを 酸化 、電子e – を得ることを 還元 という。 また、電子e – を失った物質は 「酸化された」 、電子e – を得た物質は 「還元された」 という。酸化還元反応は、酸素のやりとり、水素のやりとりだけでなく、電子e-のやりと りでも説明できます。 電子e - を失うと「酸化された」、電子e 酸化剤 1 molが受け取ることのできる電子eの数 molと、還元剤 1 molがあげることのできる電子eの数 molは、種類によって決まっています。




Woa1 フロー電池 Google Patents




Inst Quantum Beam Science 量子線科学専攻 照片 Facebook




酸化と還元のお話 本坊農園 宮崎県えびの市




化学基礎 酸化還元反応 写真の 1 が分かりません Clear



酸化還元酵素とは コトバンク




宇宙一覚えやすい 化学反応式ハンドブック Amazon Com Books



サトテック酸化還元電位計orp 3adv Orp電極sota Orp付属orp計 Buyee Buyee 提供一站式最全面最專業現地yahoo Japan拍賣代bid代拍代購服務



酸化剤と還元剤 化学基礎 高校化学net参考書



7 3 酸化剤と還元剤 おのれー Note



酸化還元反応 電子のやり取り



量子整体 ゆらぎ 科学で痛た気持ちいいとは サンクスクラブ ありがとうの力は無限大



量子力学で自然治癒力を最大に高める 還元力を上げる サンクスクラブ ありがとうの力は無限大



酸化還元反応 電子のやり取り
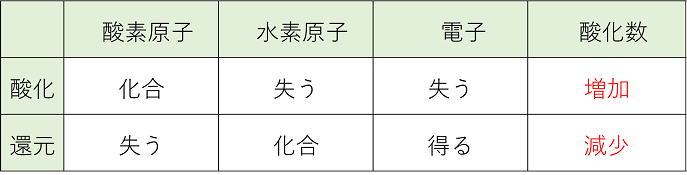



酸化と還元
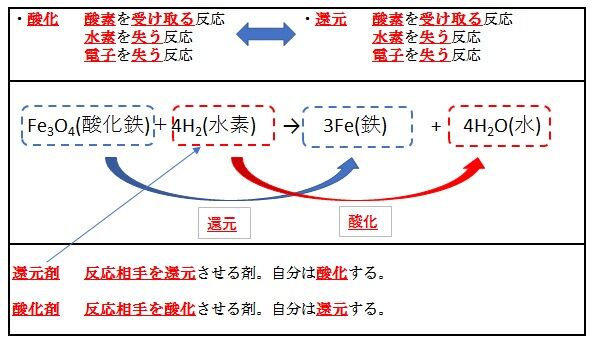



酸化還元反応について 無料で合格 危険物取扱者試験




高校化学基礎 酸化 還元と電子 映像授業のtry It トライイット




酸化還元反応



第35章 酸化と還元




高校化学基礎 酸化還元反応 酸化還元反応と電子の授受 Youtube




髭の種類 Youtube Channel Analytics And Report Powered By Noxinfluencer Mobile




還元剤 Okedic




酸化還元反応 電子のやり取り



日本中学化学 氧化与还原 哔哩哔哩 つロ干杯 Bilibili




酸化還元反応とは 反応式の書き方 コツをわかりやすく解説 高校生向け受験応援メディア 受験のミカタ




7 4 酸化還元反応の量的関係 おのれー Note




化学 酸化剤 還元剤の電子を含むイオン反応式 理論分野1 22 Youtube
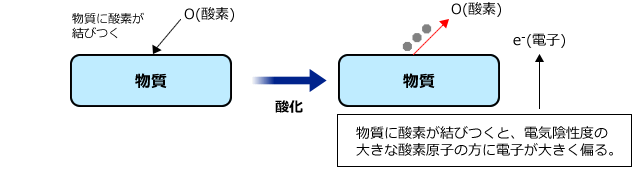



化学講座 第19回 酸化と還元 酸化 還元の定義 私立 国公立大学医学部に入ろう ドットコム



第36章 酸化剤と還元剤
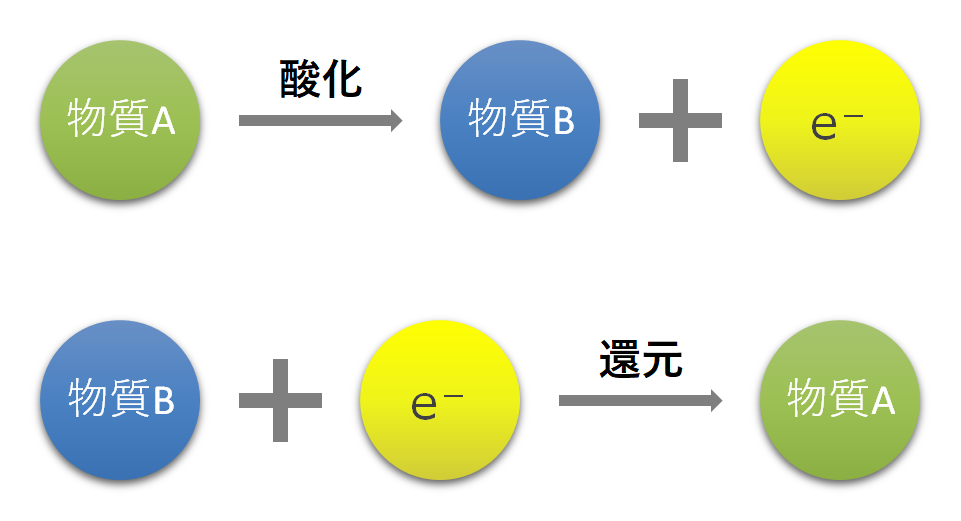



酸化と還元 酸化数から酸化還元反応を考えよう ふかラボ




高校化学基礎 酸化還元滴定の実験量的関係 映像授業のtry It トライイット



水素泡を使った洗顔 洗髪



酸化還元反応を解説 酸化数を理解して半反応式を覚えよう Studyplus スタディプラス



活性酸素 네이버 블로그




7 1 酸化と還元 おのれー Note




酸化 還元の定義について解説
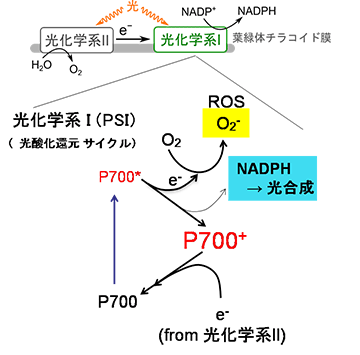



植物が活性酸素を抑制する機能の電子の流れを解明 Research At Kobe




酸化 還元反応の基本的な意味 水処理に関するご相談は 栗田工業



酸化還元反応 その3 相手の電子を奪い取り酸化させる働きを酸化作用といい 相手を酸化させる物質を酸化剤と呼びます 相手に電子を与えて還元する働きを還元 作用といい 相手を還元させる物質を還元剤と呼びます 全く別の反応で 互いに関係のない




酸化還元の定義その3とまとめ



48 6月6日 酸化 還元の基礎




代購代標第一品牌 樂淘letao 自然還元研究所hs 413dw Orpメーター酸化還元電位計



第35章 酸化と還元




Jpa 化粧品スキンケア製剤における抗酸化効果のための作用物質を同定及び評価するための転写プロファイリング及びバイオマーカーに基づく方法 Google Patents



7 1 酸化と還元 おのれー Note




どっちが酸化 還元 原理から酸化と還元を理解しよう




酸化と還元 酸素 水素 そして電子のやり取り 図解でわかる危険物取扱者講座



基礎化学4 酸 塩基 塩と酸化還元反応
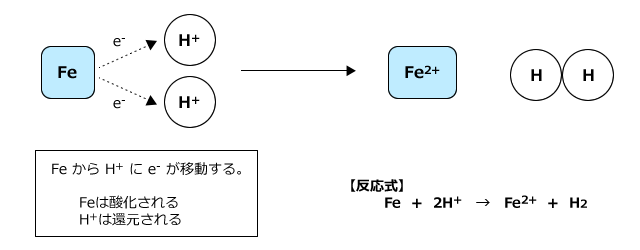



化学講座 第19回 酸化と還元 酸化 還元の定義 私立 国公立大学医学部に入ろう ドットコム



第35章 酸化と還元




化学基礎232a 化学35 13 酸化剤は相手の物質から電子を奪ってを酸化させ自分は還元され 還元剤は相手の物質に電子を与えて還元させ自分は酸化 されることは酸化数の増減を見ながら確認 Youtube



酸化と還元 活性酸素と抗酸化物質 そして酸化型coq10と還元型coq10 株式会社シクロケムバイオ



還元電子 株式会社 Erum Science イルムサイエンス




酸化還元反応 電子を含むイオン反応式 化学基礎 定期テスト対策サイト
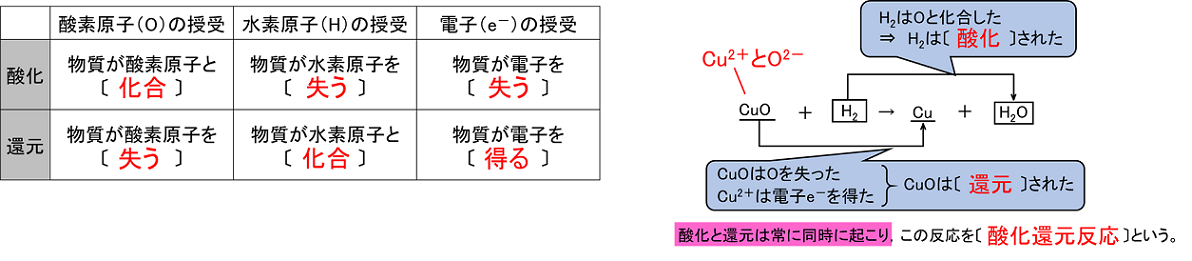



酸化と還元
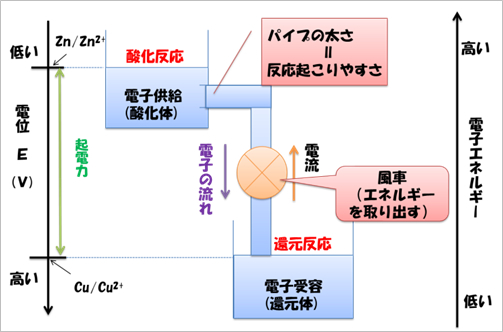



酸化還元反応の身の回りへの応用 亜鉛めっき をとおして 化学授業実践記録 アーカイブ一覧 理科 高等学校 知が啓く 教科書の啓林館




波動共鳴分析機とは サンクスクラブ ありがとうの力は無限大
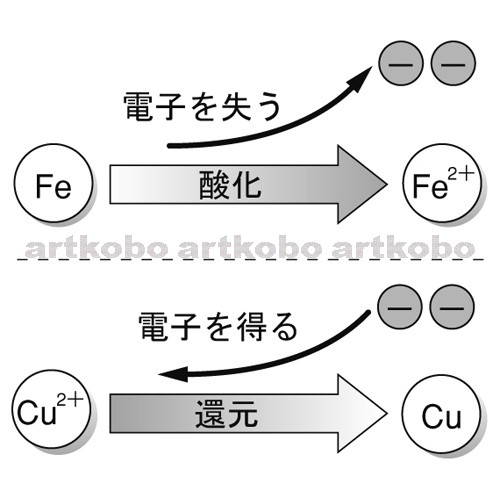



Web教材イラスト図版工房 R Ch 酸化還元反応 03




酸化還元反応 電子のやり取り




高校化学 酸化還元 酸化 還元とは オンライン無料塾 ターンナップ Youtube



酸化還元滴定
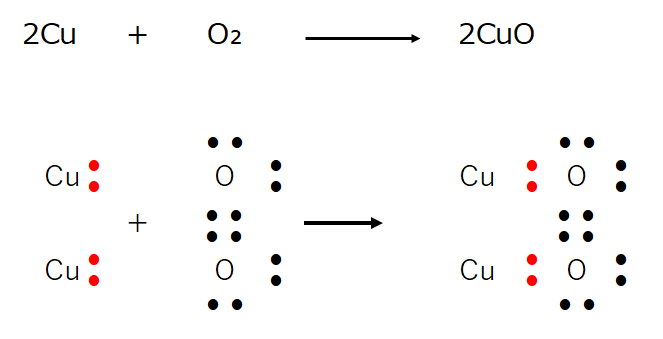



酸化還元反応 電子のやり取り



Fentons Reaction Fe Iih 2 O 2h 2
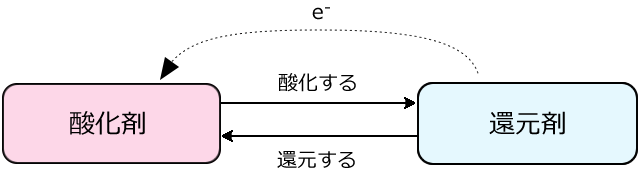



化学講座 第21回 酸化と還元 酸化剤と還元剤 酸化還元反応式 私立 国公立大学医学部に入ろう ドットコム




生体内のレドックス 酸化還元 反応と活性酸素種 生物学科 東邦大学
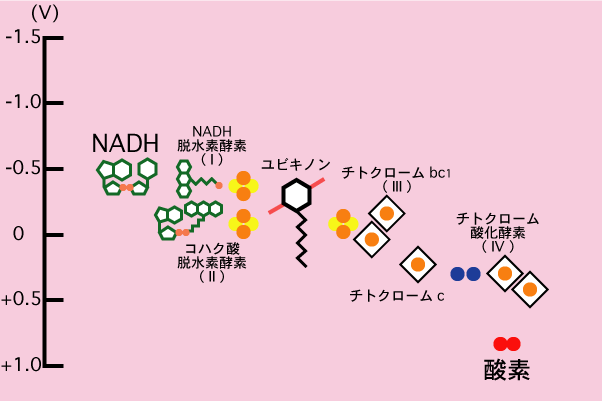



酸化還元電位




酸化還元反応の量的関係の問題についてです Clear




酸化還元反応 定義と電子の授受




6 2 酸化 還元とは 電子の受け渡し 高校生 化学のノート Clear



酸化数 Okedic



第35章 酸化と還元




書けて欲しい半反応式 1 化学がちょっとだけ好きな社労士



抗酸化力について考える なるほど元気倶楽部
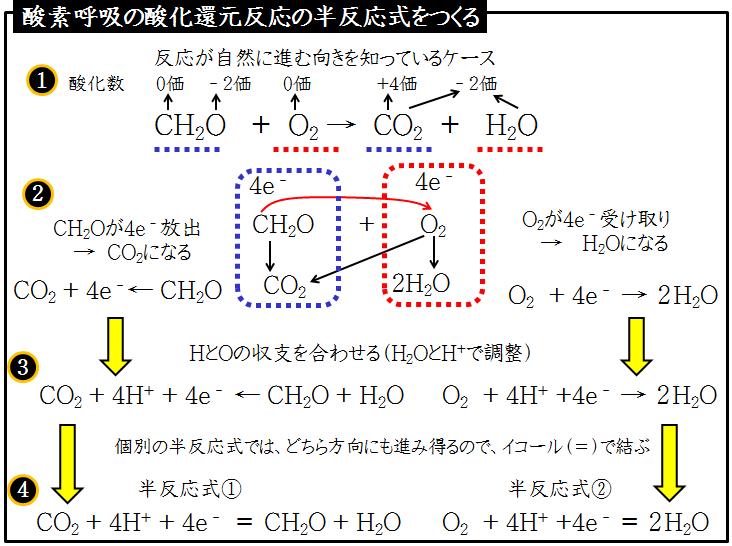



コース 酸化還元反応 半反応式の作り方 呼吸反応




光と電気化学 励起による酸化還元力の向上
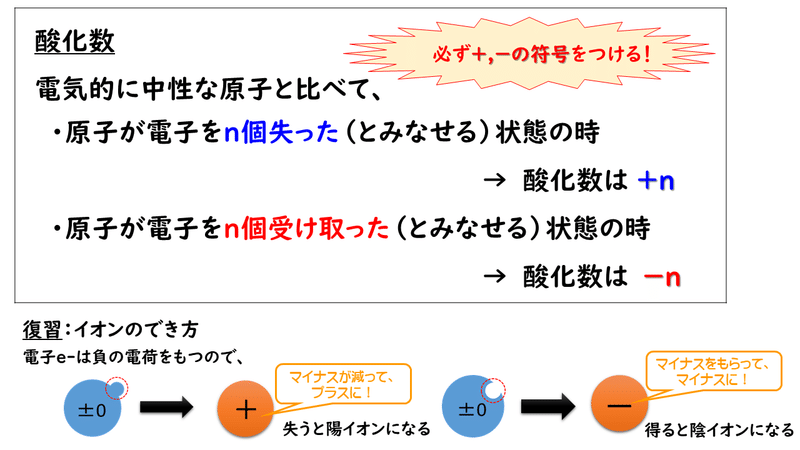



7 2 酸化数 おのれー Note




高校化学基礎 還元剤とは 映像授業のtry It トライイット




30 酸化剤と還元剤 Youtube
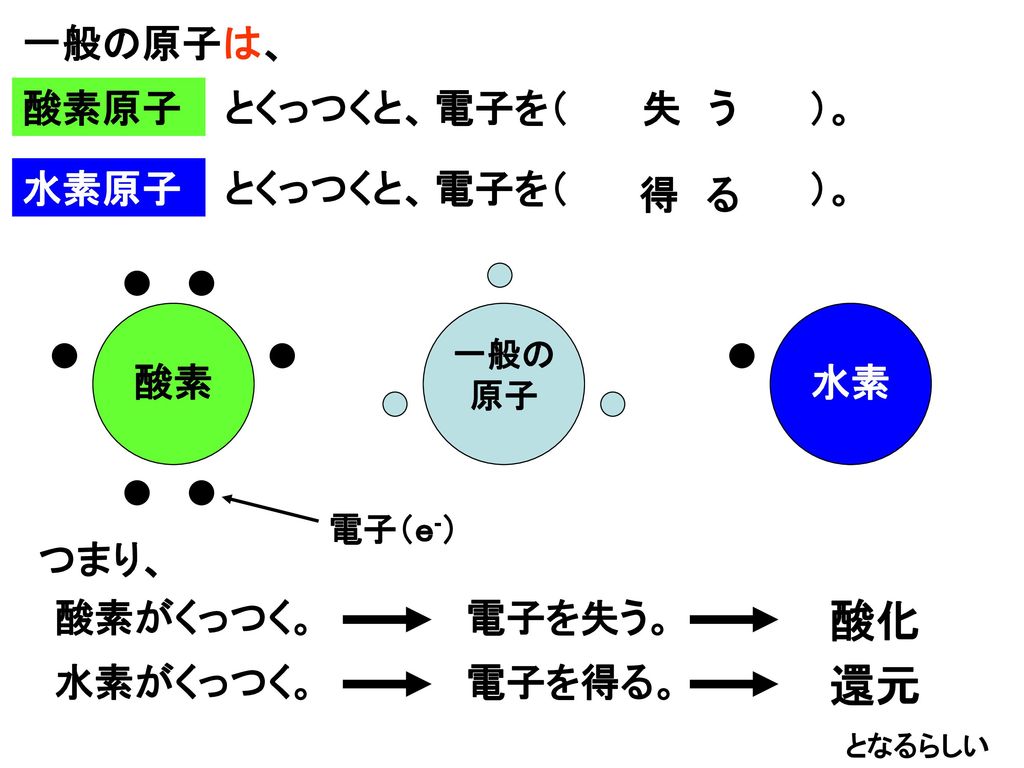



サフラニンとメチレンブルーの 酸化還元反応を利用 Ppt Download
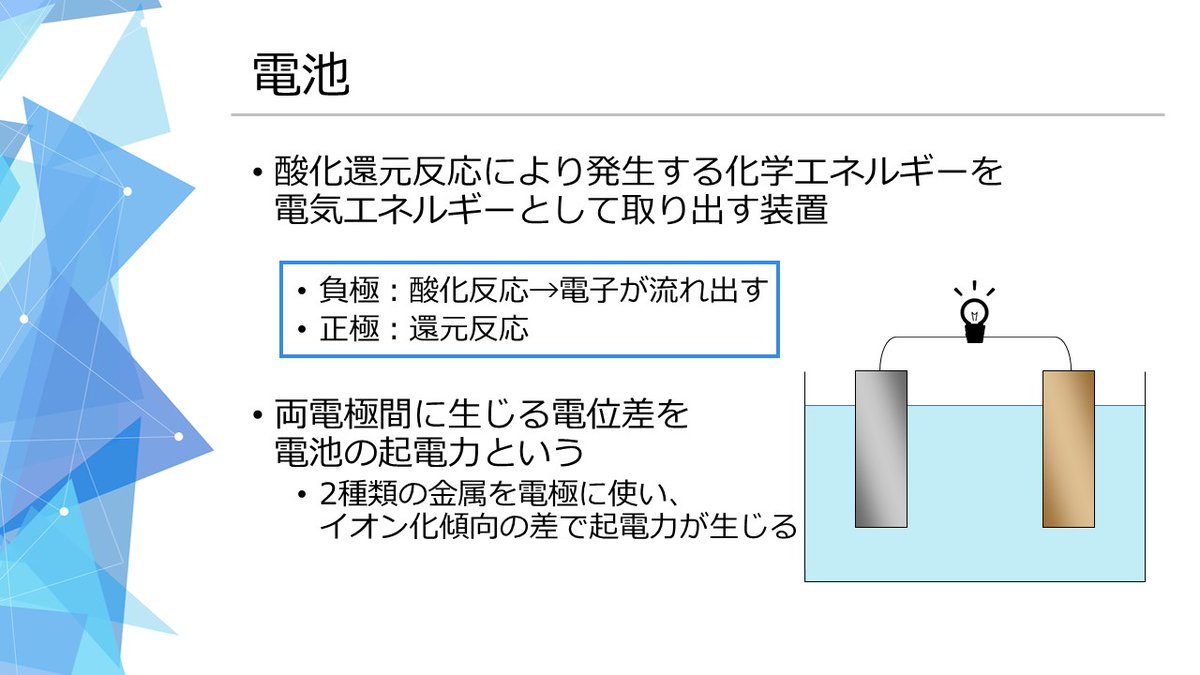



マナの勉強studio Ar Twitter 電池 酸化還元反応の応用例です 負極で酸化反応がおこり 電子が流れ出して正極で還元反応がおこります 化学基礎 センター試験 大学入学共通テスト




酸化還元反応式の作り方 理系ラボ
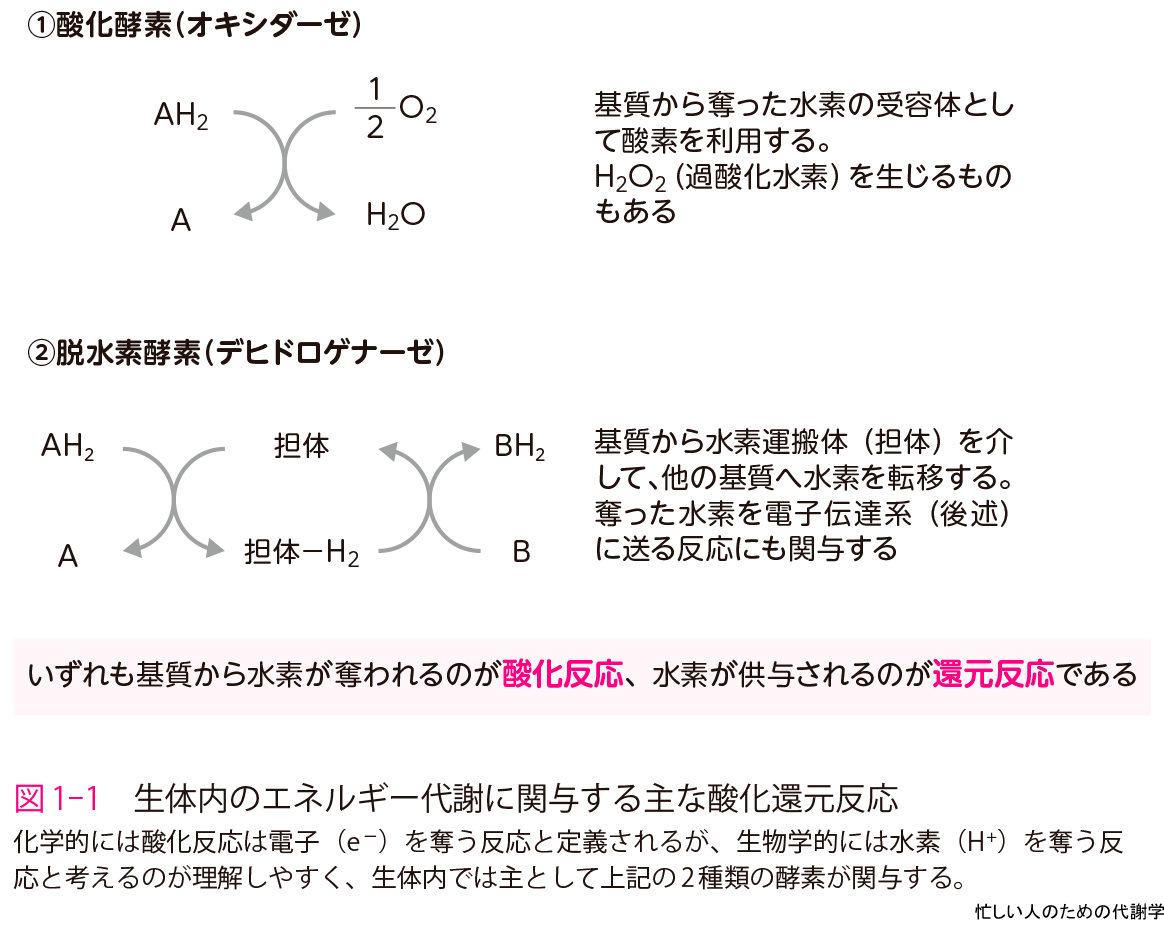



忙しい人のための代謝学 ミトコンドリアがわかれば代謝がわかる 羊土社




Senior High化学的化学基礎総復習ノートまとめ筆記 Clear
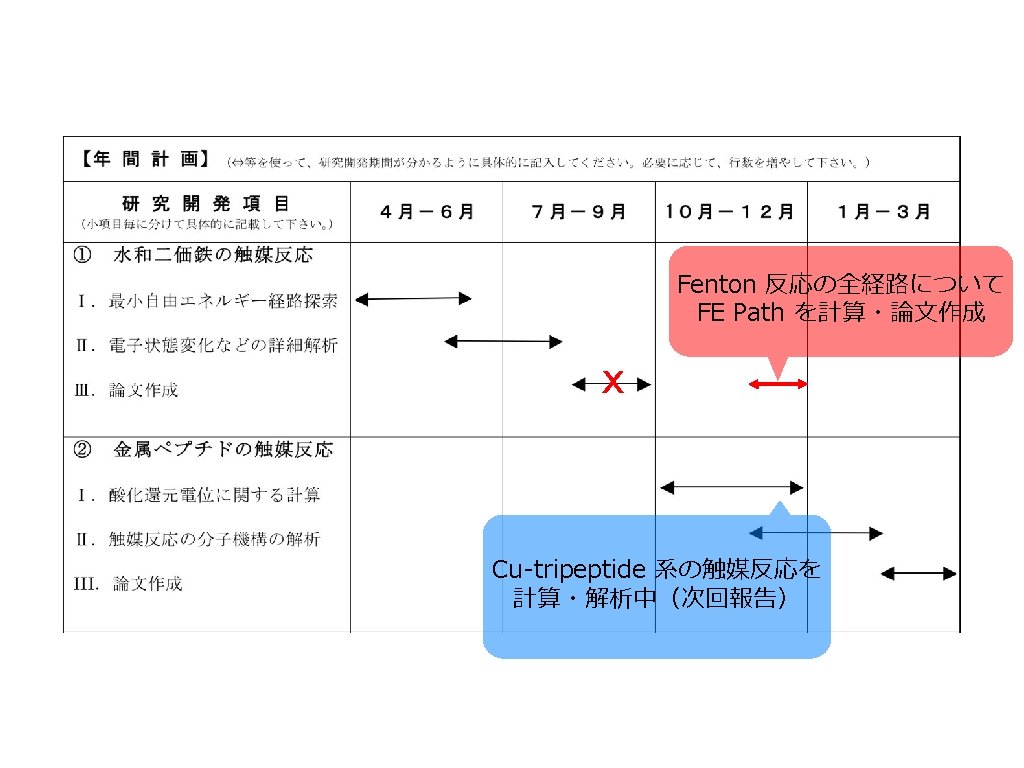



From Fenton Reagent To Oxidants Fe Ivo 2h
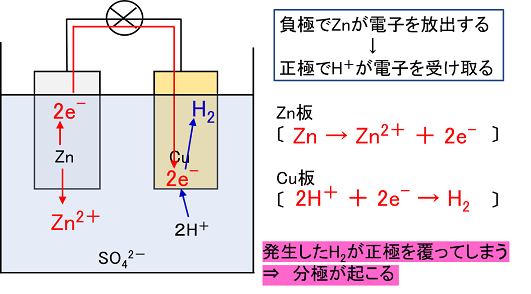



酸化還元反応の利用 電池と電気分解



受験基礎化学 26 酸化還元反応 みかみの参考書ブログ




酸化還元反応 電子のやり取り




この問題の解説お願いします 電子のやりとりによる酸化 還元の見分け方がよく分からない Clear




フレッシュ水素水粒 酸化還元電位測定 Youtube
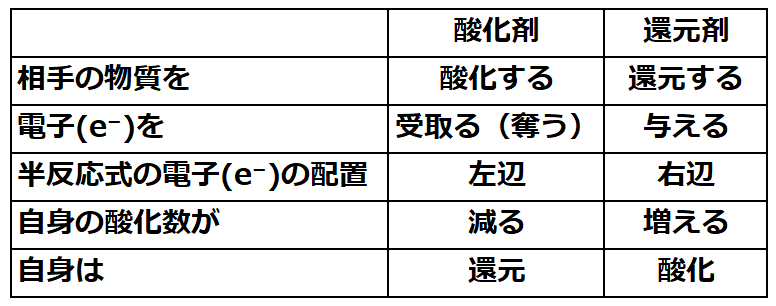



酸化還元反応 電子のやり取り




Senior High化学的化学基礎総復習ノートまとめ筆記 Clear




高校化学 酸化還元と酸化数 Youtube



酸化還元




酸化還元反応 電子のやり取り
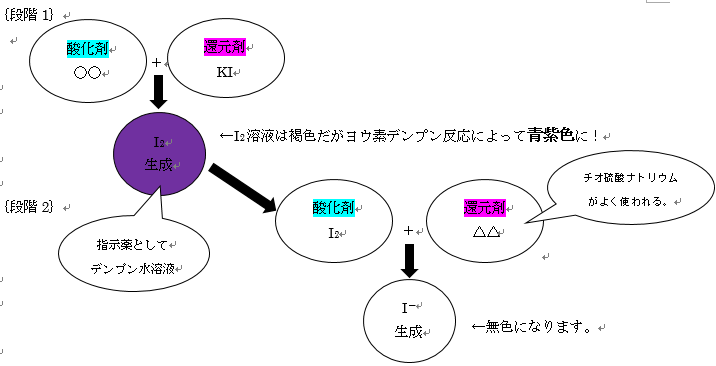



酸化還元反応とは 覚え方と式の作り方 ヨウ素滴定とは わかりやすく解説 受験の相談所
コメント
コメントを投稿